|
|
|
| 中国海洋大学在纳米材料“蛋白冠”的原位表征研究领域取得系列进展 |
| http://www.huaue.com 2024年10月5日 来源:华禹教育网 |
|
近日,中国海洋大学医药学院、海洋药物教育部重点实验室姜帅课题组在蛋白冠的原位表征研究领域取得重要进展,分别在领域内国际顶级期刊Nano
Letters和Chemical Society Reviews发表题为“In situ measurement
of nanoparticle-blood protein adsorption and its
heterogeneity with single-nanoparticle resolution via
dual fluorescence
quantification”(单纳米粒子双荧光定量法原位测定纳米颗粒-血液蛋白吸附及其非均质性)和“In
situ characterization techniques of protein corona
around nanomaterials”(纳米材料周围蛋白冠的原位表征技术)的系列研究成果。
根据蛋白冠与材料表面亲和力的不同,主要分为软冠(外层,松散结合)和硬冠(内层,紧密结合)两种类型,其中软冠直接与生物环境接触,决定纳米材料体内命运。由于软冠与材料表面结合较弱且与游离蛋白存在动态交换,对其进行准确捕捉和表征存在较大挑战。姜帅课题组基于纳米流式检测技术,开发了一种可在单颗粒水平上原位定量检测纳米−蛋白吸附的分析方法,成功定量检测了人血清白蛋白和转铁蛋白在聚苯乙烯纳米颗粒表面的吸附情况,并揭示了不同颗粒之间蛋白吸附的异质性。该项技术实现了对血清环境中纳米颗粒聚集状态和蛋白质吸附动力学的原位定量监测,未来有望应用于体内实验前的纳米药物稳定性和疗效的预评估过程(图1)。
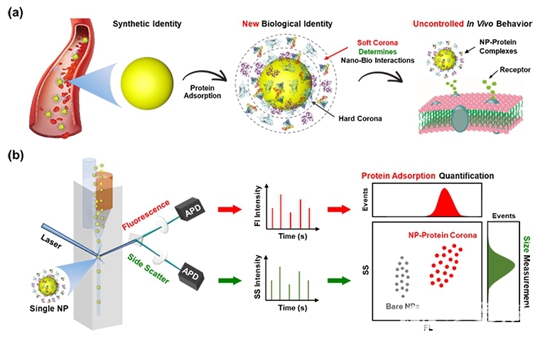
图1.(a)纳米颗粒表面蛋白冠的形成及生物学效应影响的示意图,(b)利用纳米流式检测技术在单颗粒水平上原位检测纳米颗粒-血液蛋白相互作用
研究人员进一步对蛋白冠分离技术和原位表征方法的研究进展进行了系统综述。围绕离心法、磁性分离法和色谱法等不同分离机制,首先对现有蛋白冠分离技术进行了系统分类。针对蛋白冠的原位表征方法进行了详细梳理与讨论,包括纳米颗粒尺寸变化、纳米-蛋白冠复合物的形貌表征、纳米-蛋白相互作用的动力学以及蛋白质构象变化等方面(图2)。该文章全面总结并系统分析了蛋白冠原位表征技术的优缺点及适用领域,强调了蛋白冠原位表征的重要挑战,并探讨了其对纳米药物开发和临床转化的重要意义。
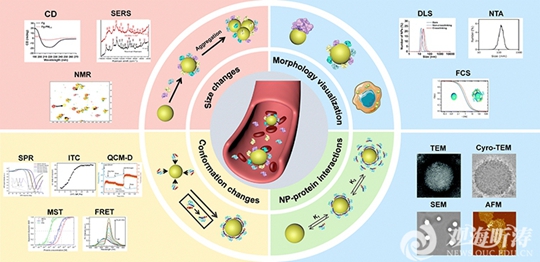
图2.用于分析纳米颗粒-血液蛋白相互作用的原位表征技术
中国海洋大学为上述两篇文章的第一完成单位,姜帅教授和德国马普高分子所Katharina Landfester教授为两篇论文的共同通讯作者,中国海洋大学博士研究生牛圆圆和付芳琴分别为两篇论文的第一作者,相关工作得到了国家自然科学基金、山东省自然科学基金等项目的支持。

姜帅课题组合影(二排中间为姜帅老师)
文章链接:
https://pubs.acs.org/doi/10.1021/acs.nanolett.4c01469
https://pubs.rsc.org/en/content/articlelanding/2024/cs/d4cs00507d
|
 关于中国海洋大学更多的相关文章请点击查看 关于中国海洋大学更多的相关文章请点击查看  |
|
| 特别说明:由于各方面情况的不断调整与变化,华禹教育网(Www.Huaue.Com)所提供的信息为非商业性的教育和科研之目的,并不意味着赞同其观点或证实其内容的真实性,仅供参考,相关信息敬请以权威部门公布的正式信息为准。 |
|
|
|
| |